Очистка воды: железо

Наиболее распространенный минерал в земной коре - это железо, и поэтому он наиболее часто встречается в воде из скважин. В подземных водах железо чаще всего встречается в виде растворенного двухвалентного железа Fe2+, а в поверхностных водах — в виде комплексных соединений либо в виде коллоидных или тонкодисперсных взвесей. Согласно СанПиН 2.1.4.1074-01 "Питьевая вода", допустимый уровень железа в воде составляет 0,3 мг/л.
Анаэробная (не имеющая контакта с воздухом) прозрачная грунтовая вода может содержать соединения двухвалентного железа (Fe2+) до нескольких миллиграммов на литр без ее помутнения при прямой подаче из источника. Однако при контакте с воздухом, а точнее, с кислородом воздуха, двухвалентное железо окисляется до трехвалентного коллоидного состояния, придавая воде характерный красно-коричневый оттенок.
Содержание железа в воде выше норматива способствует накоплению осадка в системе водоснабжения, интенсивному окрашиванию сантехнического оборудования. При значениях более 0,3 мг/л железо оставляет пятна на белье при стирке. Железо придает воде неприятную красно-коричневую окраску, ухудшает ее вкус, вызывает развитие железобактерий, отложение осадка в трубах и их засорение. Высокое содержание железа в воде приводит к неблагоприятному воздействию на кожу, способствует возникновению аллергических реакций.
Для питьевых целей применяются, в основном, подземные воды. Качество подземных вод Томской области по ряду таких показателей как содержание железа, марганца, кремния, а в отдельных случаях фенолов, азотсодержащих веществ, нефтепродуктов, сероводорода, метана, не отвечает требованиям СанПиН 2.1.4.1074-01 "Питьевая вода".
Основная проблема использования подземных вод в Томской области заключается в высоком содержании в них растворенных соединений железа, что в значительной мере связано с влиянием природных факторов, особую роль среди которых играет сильная заболоченность территории области. Железо в подземной воде содержится в виде двухвалентного иона Fe2+. Использование воды такого состава требует специальной водоподготовки, включающей аэрацию для перевода Fe2+ в трехвалентное железо Fe3+, отстаивание и фильтрование.
Железо в скважинах находится в растворенной форме, поэтому на первый взгляд вода кажется абсолютно чистой и прозрачной. Но если она какое-то время постоит на воздухе, то начинает приобретать рыжий цвет - железо переходит в окисленную форму.
Существует большое количество способов удаления железа, а именно:
1) Аэрация воды с последующим ее фильтрованием или отстаиванием и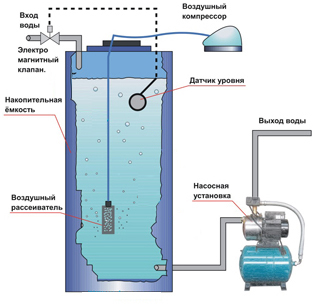 фильтрованием. Аэрация представляет собой обработку водного потока воздухом, при котором происходит окисление растворенных соединений железа кислородом воздуха и переведение их в окисленную форму, образующую хлопьевидный осадок, легко задерживаемый засыпными осадочными фильтрами. Также при аэрации происходит отдувка из воды летучих примесей, в том числе токсичных и обладающих неприятным запахом, например сероводорода;
фильтрованием. Аэрация представляет собой обработку водного потока воздухом, при котором происходит окисление растворенных соединений железа кислородом воздуха и переведение их в окисленную форму, образующую хлопьевидный осадок, легко задерживаемый засыпными осадочными фильтрами. Также при аэрации происходит отдувка из воды летучих примесей, в том числе токсичных и обладающих неприятным запахом, например сероводорода;
2) Коагулирование, осветление, флокулирование. В воду добавляют химические реагенты - так называемые коагулянты, которые, вступая в реакцию с содержащимися в воде солями, способствуют осаждению взвешенных и коллоидальных частиц. Для интенсификации процесса коагуляции в воду дополнительно вводят флокулянты. Флокулянты способствуют укрупнению осадка и ускоряют процесс слипания осаждаемых коллоидных и взвешенных частиц;
3) Известкование. Применяют с целью удаления сернокислого железа, которое в результате реакции образует в начале гидрат закиси, а затем при контакте с кислородом - гидрат окиси;
4) Введение реагентов-окислителей.
Обработка воды хлором и его производными. Под действием хлора происходит разрушение гуматов и других органических соединений железа и переход их в форму неорганических солей трехвалентного железа, которые легко гидролизуются. В результате гидролиза выпадает осадок или гидроксида железа, или продуктов неполного гидролиза – основных солей железа различного состава.
Обработка воды перманганатом калия. Метод окисления двухвалентного железа используется путем введения в исходную воду перед фильтрами раствора перманганата калия KMnO4. Последний может также вводиться в сочетании с гипохлоритом натрия с целью обработки сложных вод и экономии перманганата калия –достаточно дорогостоящего окислителя.
Обработка воды озоном. Один из перспективных методов окисления железа – озонирование. Озон (О3) – один из самых сильных окислителей. Одновременно с обеззараживанием идут процессы окисления двухвалентных железа и марганца, обесцвечивание воды, а также ее дезодорация и улучшение органолептических свойств.
5) Фильтрование с применением каталитических загрузок.
Фильтрование с применением каталитических загрузок – наиболее распространенный метод удаления железа и марганца, применяемый в высокопроизводительных компактных системах. Это обусловлено как коммерческими аспектами, так и высокой технологичностью процессов. Каталитические наполнители – природные материалы, содержащие диоксид марганца или загрузки, в которые диоксид марганца введен при соответствующей обработке: дробленый пиролюзит, «черный песок», сульфоуголь и МЖФ (отечественные загрузки); Manganese Green Sand (MGS), 
 Birm, МТМ (зарубежные наполнители);
Birm, МТМ (зарубежные наполнители);
Эти фильтрующие «засыпки» отличаются друг от друга как своими физическими характеристиками, так и содержанием диоксида марганца и поэтому эффективно работают в разных диапазонах значений характеризующих воду параметров. Однако принцип их работы одинаков. Механизм действия основан на способности соединений марганца сравнительно легко изменять валентное состояние. Двухвалентное железо в исходной воде окисляется высшими оксидами марганца. Последние восстанавливаются до низших ступеней окисления, а далее вновь окисляются до высших оксидов растворенным кислородом и перманганатом калия.

 Впоследствии большая часть окисленного и задержанного на фильтрующем материале железа вымывается в дренаж при обратной промывке. Таким образом, слой гранулированного катализатора служит одновременно и фильтрующей средой. Для улучшения процесса окисления в воду могут добавляться дополнительные химические окислители. При проведении процесса следует иметь в виду, что для эффективного окисления соединений железа (и марганца) необходимо как наличие катализатора, который только ускоряет процесс, так и реагента-окислителя. В роли последнего может выступать растворенный кислород, высшие соединения марганца, хлор, гипохлорит. С этой точки зрения разделение методов обезжелезивания (на реагентные и безреагентные) носит условный характер. В любом случае в ходе реакции расходуется окислитель независимо от того, вводится он извне или входит в состав фильтрующей загрузки. В последнем случае следует определить ресурс загрузки, исходя из состава воды и ее расхода, а также обеспечить своевременную регенерацию или замену фильтрующего материала.
Впоследствии большая часть окисленного и задержанного на фильтрующем материале железа вымывается в дренаж при обратной промывке. Таким образом, слой гранулированного катализатора служит одновременно и фильтрующей средой. Для улучшения процесса окисления в воду могут добавляться дополнительные химические окислители. При проведении процесса следует иметь в виду, что для эффективного окисления соединений железа (и марганца) необходимо как наличие катализатора, который только ускоряет процесс, так и реагента-окислителя. В роли последнего может выступать растворенный кислород, высшие соединения марганца, хлор, гипохлорит. С этой точки зрения разделение методов обезжелезивания (на реагентные и безреагентные) носит условный характер. В любом случае в ходе реакции расходуется окислитель независимо от того, вводится он извне или входит в состав фильтрующей загрузки. В последнем случае следует определить ресурс загрузки, исходя из состава воды и ее расхода, а также обеспечить своевременную регенерацию или замену фильтрующего материала.
Все системы на основе каталитического окисления с помощью диоксида марганца имеют ряд ограничений:
-неэффективны в отношении органического железа; более того, при наличии в воде любой из форм органического железа, на поверхности гранул фильтрующего материала со временем образуется органическая пленка, изолирующая катализатор (диоксид марганца) от воды;
- не могут справиться со случаями, когда содержание железа в воде превышает 10–15 мг/л, что совсем не редкость. Присутствие в воде марганца еще более ухудшает эффективность обезжелезивания.